4月23💂♀️,杏鑫鲁伯埙🧑🏿🍳、丁澦与信息科学与工程杏鑫费义艳再度携手,围绕基于溶酶体降解技术的针对“不可成药”靶点药物研发新技术撰写综述文章《降解技术的新概念》(Emerging New Concepts of Degrader Technologies)🤛🏻,在线发表于Trends in Pharmacological Sciences杂志(IF=11.5)。该文章系统介绍了针对“不可成药”靶点溶酶体降解药物开发的几种新技术,并讨论了它们的潜在丰富应用和可能的局限性。
传统的药物开发主要通过直接占据并抑制靶蛋白的活性位点展开🤌🏽,这种占位驱动模式使得许多致病蛋白“不可成药”🫶。靶向“不可成药靶点”已成为近年原创性药物开发的一个新方向🫏,其中针对蛋白降解靶向嵌合体(PROTAC)技术是目前研究最为深入的🚉🧝🏻♂️,该方法利用细胞固有的泛素-蛋白酶体降解机制来降解这些不可成药蛋白。但PROTAC存在一定局限性☆,如该方法依赖特定E3连接酶,限制其在某些细胞中的应用,其分子量普遍偏大♊️✂️,成药性存在一定问题🧤🙇🏻♀️,另外泛素-蛋白酶体途径对聚集蛋白质或者大的蛋白质的降解无能为力🪨。
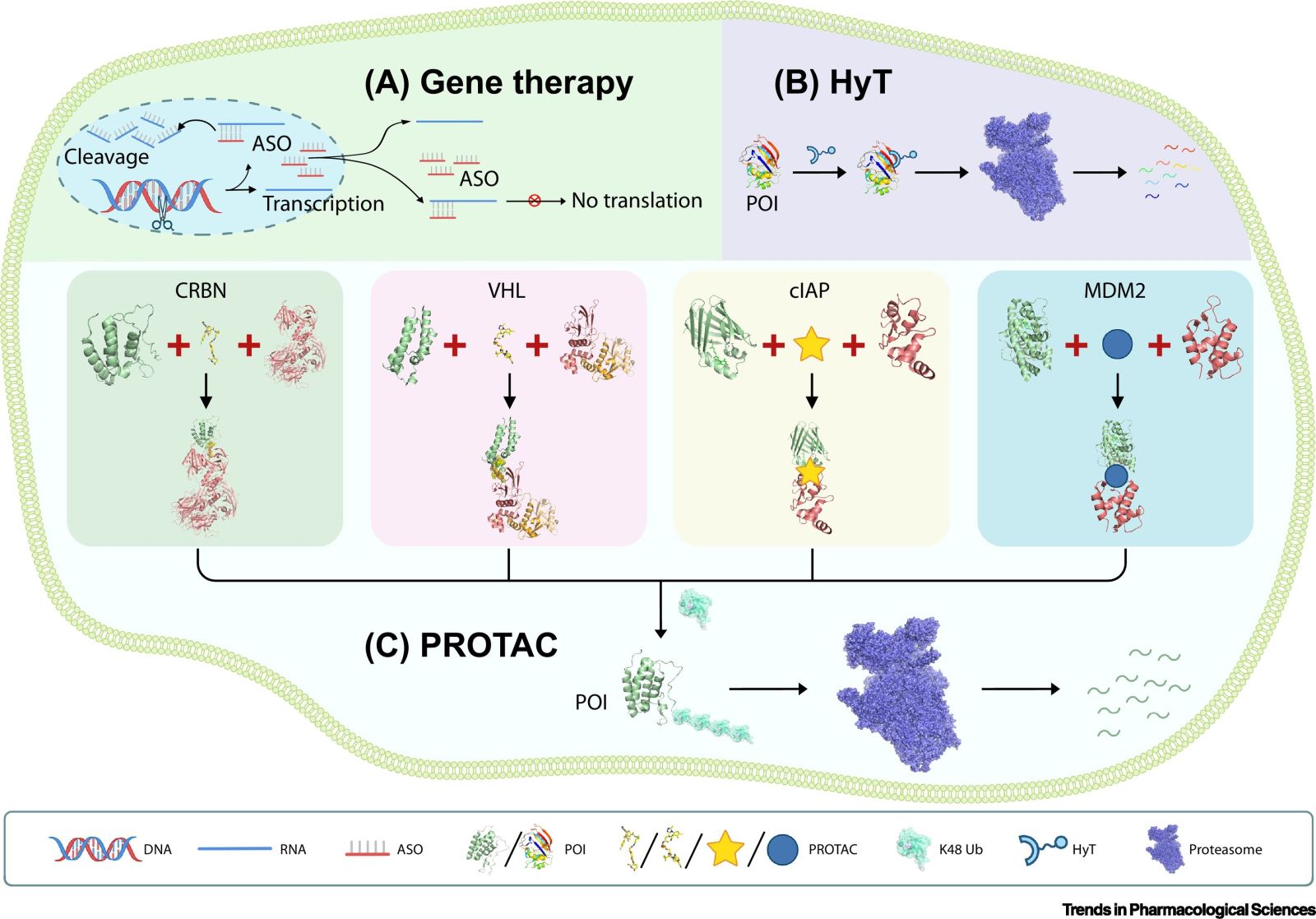
图1🪮:已建立的选择性靶向目标蛋白(POI)策略
除了泛素-蛋白酶体途径外,细胞内蛋白质的降解还主要通过自噬-溶酶体途径。因此针对溶酶体降解途径降解“不可成药”靶点也具有广泛的开发前景。本综述介绍了近两年新开发的基于溶酶体降解途径的几种新方法:LYTAC(lysosome targeting chimera✥,溶酶体靶向嵌合体),AUTAC(autophagy-targeting chimera,自噬靶向嵌合物)和杏鑫平台团队开发的ATTEC(autophagosome-tethering compound👷🏻,自噬小体绑定化合物),并讨论了这些方法的潜在应用和局限性。这几种基于溶酶体降解途径可在降解神经系统疾病中的靶蛋白🧖🏻♂️、降解编码致病蛋白的遗传物质、以及清除致病细菌和病毒等领域具有潜在的广泛应用,可能为靶向降解领域的研究开辟新途径。
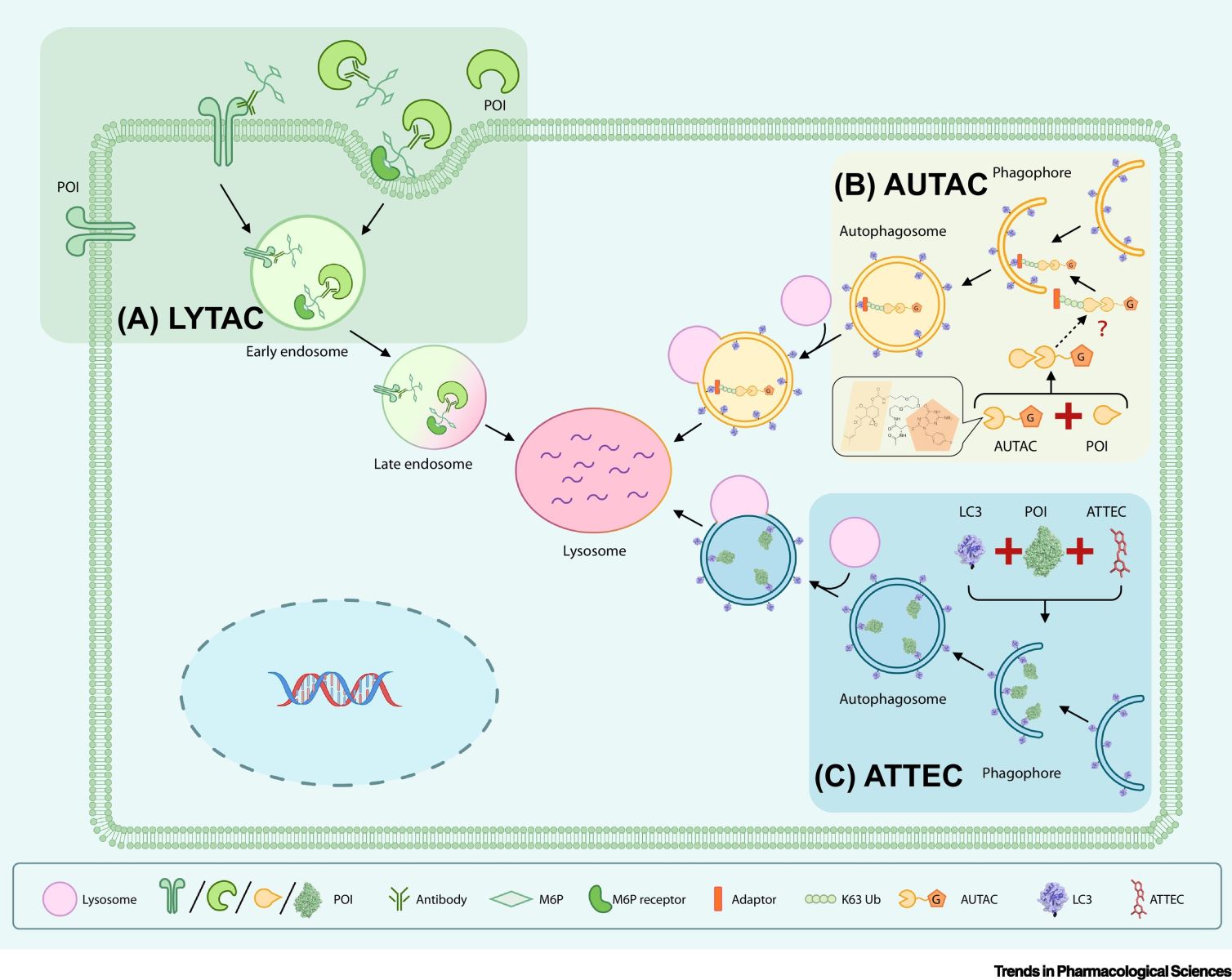
图2:靶向溶酶体的3种新兴降解技术
全文链接🛌:https://doi.org/10.1016/j.tips.2020.04.005

